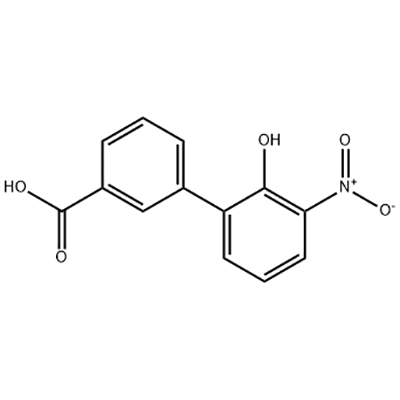
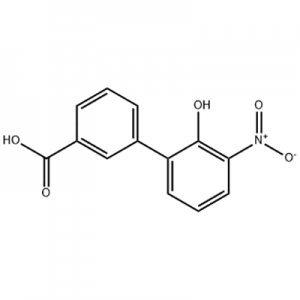
2′-hydroxy-3′-nitro-3-biphenylcarboxylic acid
2′-hydroxy-3′-nitro-3-biphenylcarboxylic acid
2'-hydroxy-3'-nitro-3-biphenylcarboxylic acid Eltrombopag को मध्यवर्ती रूपमा प्रयोग गरिन्छ।
एल्ट्रोम्बोपाग, ग्लैक्सोस्मिथक्लाइन (GSK) द्वारा बेलायतमा विकसित र पछि स्विट्जरल्याण्डमा नोभार्टिससँग संयुक्त रूपमा विकसित, विश्वको पहिलो र एकमात्र स्वीकृत सानो अणु गैर पेप्टाइड TPO रिसेप्टर एगोनिस्ट हो।इडियोपैथिक थ्रोम्बोसाइटोपेनिक परपुरा (ITP) को उपचारको लागि र 2014 मा गम्भीर अप्लास्टिक एनीमिया (AA) को उपचारको लागि अमेरिकी FDA द्वारा Eltrombopag लाई 2008 मा अनुमोदन गरिएको थियो।यो हालैका ३० वर्षमा AA को उपचारको लागि US FDA द्वारा अनुमोदित पहिलो औषधि पनि हो।
डिसेम्बर २०१२ मा, यूएस FDA ले क्रोनिक हेपाटाइटिस सी (CHC) भएका बिरामीहरूमा थ्रोम्बोसाइटोपेनियाको उपचारको लागि Eltrombopag लाई अनुमोदन गर्यो, ताकि कम प्लेटलेट काउन्टको कारण हेपाटाइटिस C रोगीहरूले कलेजो रोगहरूको लागि इन्टरफेरोन आधारित मानक थेरापी सुरु गर्न र कायम राख्न सकून्।फेब्रुअरी 3,2014 मा, GlaxoSmithKline ले घोषणा गर्यो कि FDA ले इम्युनोथेरापीलाई पूर्ण रूपमा प्रतिक्रिया नगर्ने गम्भीर केमिकलबुक एप्लास्टिक एनीमिया (SAA) भएका बिरामीहरूमा हेमोपेनियाको उपचारको लागि Eltrombopag को सफल उपचार औषधि योग्यता प्रदान गरेको छ।24 अगस्त, 2015 मा, अमेरिकी FDA ले क्रोनिक इम्यून थ्रोम्बोसाइटोपेनिया (ITP) भएका वयस्कहरू र 1 वर्ष वा माथिका बच्चाहरूमा थ्रोम्बोसाइटोपेनियाको उपचारको लागि Eltrombopag लाई अनुमोदन गर्यो जसको कोर्टिकोस्टेरोइड्स, इम्युनोग्लोबुलिन वा स्प्लेनेक्टोमीमा अपर्याप्त प्रतिक्रिया छ।जनवरी 4, 2018 मा, Eltrombopag लाई चीनमा प्राथमिक प्रतिरक्षा थ्रोम्बोसाइटोपेनिया (ITP) को उपचारको लागि सूचीबद्ध गर्न अनुमोदन गरियो।


![Casp ungin एसीटेट; Caspofungin एसीटेट; Cancidas; Caspofungin एसीटेट [USAN: BAN: JAN];](http://cdn.globalso.com/jindunchem-med/fbe17385-300x300.jpg)


![2-butyl-5-nitro-3-benzofuranyl)[4-[3-(dibutylaMino)propoxy]फिनाइल]](http://cdn.globalso.com/jindunchem-med/922e79ba.jpg)
